نقد و بررسی
کیت الیزا HIV-Ab (نسل چهارم) – پیشتاز طبکیت الایزای HIV شرکت پیشتاز طب یک محصول پیشرفته برای شناسایی آنتیبادیهای اختصاصی ویروس نقص ایمنی انسانی (Human Immunodeficiency Virus – HIV) در نمونههای سرم یا پلاسمای خون است. این کیت برای تشخیص زودهنگام عفونت HIV کاربرد دارد و به ویژه در غربالگری بیماران و پایش سلامت افراد در معرض خطر اهمیت دارد. طراحی این کیت بر اساس فناوریهای مدرن و مطابق با استانداردهای بینالمللی، دقت و حساسیت بالایی را در ارائه نتایج تضمین میکند. کیت الایزای HIV شرکت پیشتاز طب ابزاری قابل اعتماد برای آزمایشگاههای تشخیصی است و با سهولت در استفاده، امکان تشخیص سریع و دقیق را فراهم میسازد، که نقش مهمی در مدیریت پیشگیری و درمان بیماری HIV ایفا میکند.
مشخصات نمونه و آماده سازی بیمار
نوع نمونه
سرم
ظرف/لوله جمع آوری نمونه
ترجیحا: لوله لخته ژل دار
قابل قبول: لوله درب قرمز
ظرف/لوله ارسال: ویال پلاستیکی
حجم نمونه: 1.5 میلی لیتر
دستورالعمل های جمع آوری: سانتریفیوژ کنید و سرم را در ویال پلاستیکی سانتریفیوژ کنید.
حداقل حجم نمونه
1.5 میلی لیتر
معیارهای رد نمونه
| مورد | نیجه |
|---|---|
| همولیز | خوب |
| لیپمی | ردکردن |
| ایکتریک | رد کردن |
اطلاعات پایداری نمونه
| نوع نمونه | درجه حرارت | زمان |
|---|---|---|
| سرم | منجمد (ترجیحاً) | 30 روز |
| سرم | محیط | 7 روز |
| سرم | در یخچال | 7 روز |
اطلاعات بالینی
داده های اپیدمیولوژیک نشان می دهد که ایدز توسط حداقل 2 نوع HIV ایجاد می شود. اولین ویروس، HIV-1، از بیماران مبتلا به ایدز یا کمپلکس مرتبط با ایدز و از افراد آلوده بدون علامت در معرض خطر بالای ایدز جدا شده است. HIV-1 از طریق تماس جنسی، قرار گرفتن در معرض خون یا فرآورده های خونی آلوده، یا از مادر آلوده به جنین یا نوزادش منتقل می شود. دومین ویروس HIV-2، از بیماران در غرب آفریقا در سال 1986 جدا شد. به نظر می رسد HIV-2 فقط در غرب آفریقا بومی است، اما در افرادی که در غرب آفریقا زندگی کرده اند یا با آنها رابطه جنسی داشته اند نیز شناسایی شده است. HIV-2 از نظر مورفولوژی، ساختار کلی ژنومی و توانایی آن در ایجاد ایدز شبیه HIV-1 است.
آنتی بادی های ضد HIV-1 و HIV-2 معمولاً تا 6 تا 12 هفته پس از مواجهه شناسایی نمی شوند و تقریباً همیشه تا 12 ماهگی شناسایی می شوند. ممکن است آنتی بادی ها در مرحله پایانی ایدز به سطوح غیرقابل تشخیص افت کنند.
تفسیر
یک نتیجه غربالگری آنتی بادی واکنش پذیر HIV-1/-2 به دست آمده توسط آنزیم ایمونواسی (EIA) وجود عفونت HIV-1 و/یا HIV-2 را نشان می دهد. با این حال، بین واکنش آنتی بادی HIV-1 و HIV-2 تفاوتی قائل نمی شود. تشخیص عفونت HIV باید بر اساس نتایج آزمایشهای تکمیلی، مانند آزمایش تأیید/تمایز آنتیبادی HIV (به طور خودکار روی همه نمونههایی که نتایج آزمایش صفحه نمایش واکنشدهنده با هزینه اضافی بازتاب میشود) باشد.
تمام نتایج احتمالی آزمایش آنتی بادی مثبت باید با ارسال نمونه سرم دوم برای آزمایش مجدد تأیید شود.
نتیجه منفی غربالگری آنتی بادی HIV-1/-2 EIA معمولاً نشان دهنده عدم وجود عفونت HIV-1 یا HIV-2 است. با این حال، برای نمونههایی که با آزمایشهای آنتیبادی سریع HIV واکنش نشان میدهند، آزمایش تأییدی توصیه میشود، حتی اگر نتایج EIA منفی باشد
نکات مهم
– ارزش پیشبینی یک تست واکنشی (یا مثبت) به شدت به شیوع عفونت در جمعیت مورد آزمایش بستگی دارد، هر چه شیوع عفونت HIV کمتر باشد، ارزش اخباری مثبت آزمایش کمتر است.
– فردی که در مطالعه واکسن HIV شرکت کرده است ممکن است آنتی بادی هایی علیه واکسن ایجاد کند و ممکن است به HIV آلوده باشد یا نباشد. ارتباط بالینی با مشاوره مناسب، ارزیابی پزشکی، و احتمالاً آزمایشات اضافی برای تصمیم گیری در مورد اینکه آیا تشخیص عفونت HIV درست است، لازم است.
– اگر بیمار علائم بالینی و/یا سابقه رفتارهای پرخطر برای عفونت HIV داشته باشد، نتایج منفی باید با احتیاط ارزیابی شود. مرکز کنترل و پیشگیری از بیماری، آزمایش تاییدی بر روی نمونههای سرمی را توصیه میکند که با تستهای آنتیبادی سریع HIV واکنشپذیر هستند، حتی اگر نتایج اولیه EIA منفی باشد.
– غربالگری و آزمایش های تاییدی برای آنتی بادی های HIV-1/-2 نمی تواند بین عفونت فعال HIV نوزادان و انتقال غیر فعال آنتی بادی های HIV مادر در نوزادان در طول دوره پس از تولد (تا سن 2 سالگی) تمایز قائل شود. نتایج آزمایش آنتی بادی مثبت و واکنشی در نوزادان در این دوره ممکن است نشان دهنده انتقال غیر فعال آنتی بادی های HIV مادر باشد. تشخیص عفونت HIV در نوزادان و نوزادان تا 2 سال باید با آزمایشات ویروس شناسی، مانند تشخیص DNA یا PCR صورت پذیرد.
– یک غربالگری مثبت و نتیجه آزمایش آنتی بادی HIV تایید شده باید توسط ارائه دهنده مراقبت های بهداشتی به وزارت بهداشت (در ایالات متحده امریکا) گزارش شود، همانطور که قانون در برخی ایالت های امریکا الزامی می کند.
مرجع: سایت Myoclinic (لینک مرجع)
محتویات کیت HIV شرکت پیشتاز طب
| Specifications | Title |
|---|---|
| Antigen Sandwich-Antibody Sandwich | Assay Type |
| Ready to use | Chromogen Substrate |
| One :concentrate(20X) (dilution1:20 with conjugate 1 diluent), number two: Ready to us | Conjugate |
| μl 50 , 100 | Required Samplers |
| min in 37⁰C 30 + 15 + 15 + 15 | Incubation time |
| Three vials: negativ , Ag positive & Ab positive | Control |
| – | Standards |
روش انجام HIV-Ab شرکت پیشتاز طب
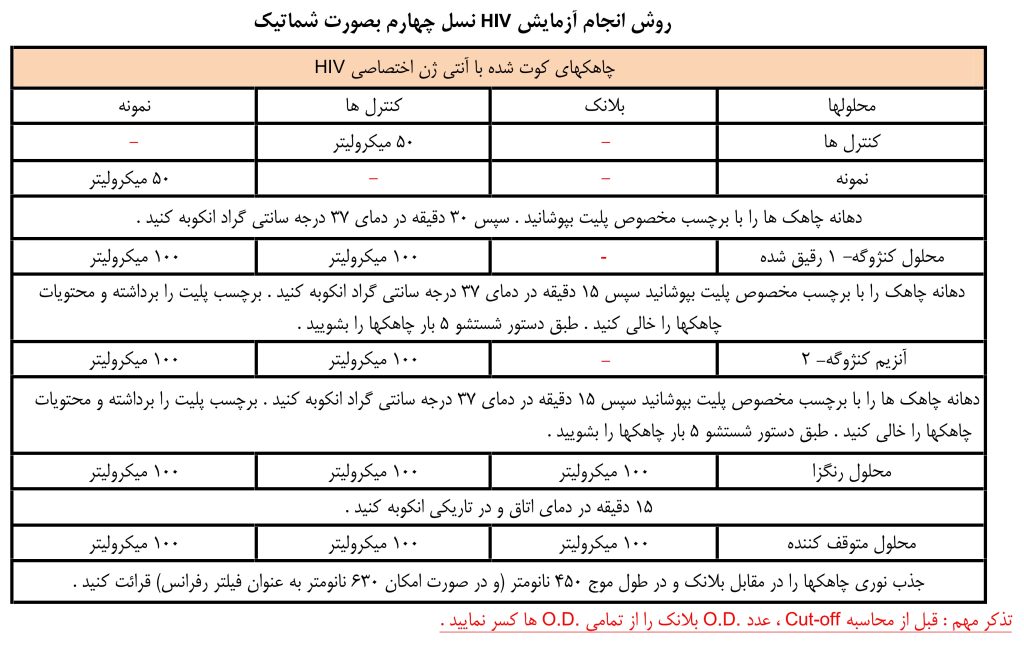



















0دیدگاه